结核病[2]又叫“痨病”,是仅次于COVID-19的第二大传染性杀手,主要通过⻜沫传播。患者可能⻓期咳嗽,咳出的黏液带血,其肺部能检测出病原菌。据估计,2022年共有130万人死于结核病,全球约有四分之一的人口已经感染结核杆菌,大约5%至10%的感染者最终会出现症状并发展为结核病,感染但尚未发病的人没有传染性。
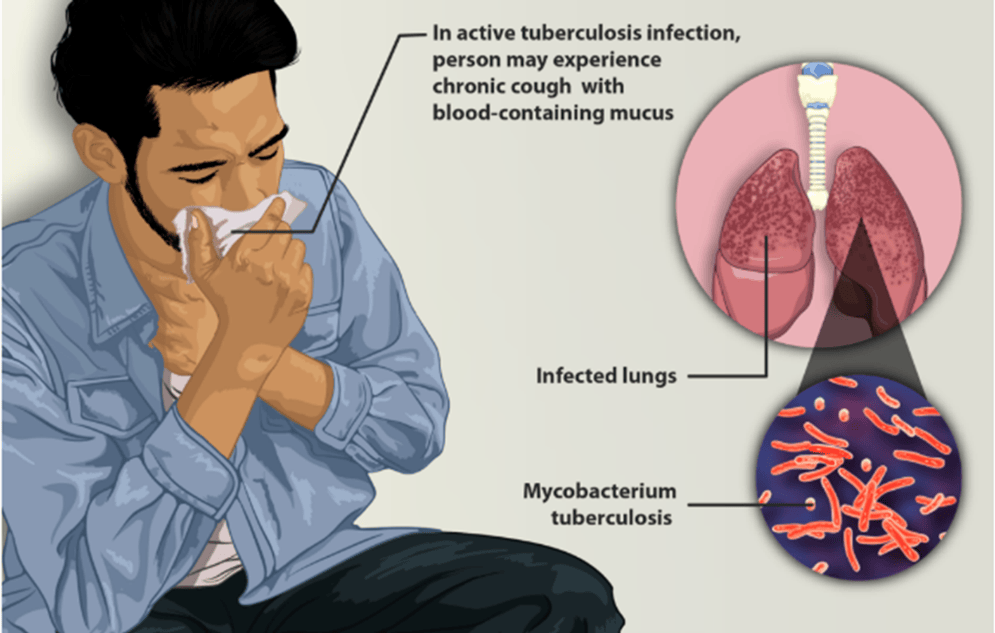
肺结核患者肺部能检测出结核分枝杆菌
引起结核病的病原菌是结核分枝杆菌(Mycobacterium tuberculosis, MTB),俗称结核杆菌(tubercle bacillus),可通过呼吸道、消化道或皮肤损伤侵入易感机体,引起多种组织器官的结核病,其中最为常⻅的是通过呼吸道引起肺结核。
结核分枝杆菌会破坏宿主细胞中的溶酶体,这是其致病能力的关键。溶酶体[3]是细胞内膜系统中的重要组成部分,这些单层膜的囊状器官内含有多种水解酶,在弱酸性环境(通常为pH值4.5-5.0)中能够有效分解和回收细胞成分,并分解被细胞内化的细菌和病毒,有助于清除异物并保持细胞内环境的稳定。然而,如果溶酶体膜因物理应激、化学损伤或病原体而受损,水解酶的释放可能会降解细胞成分或引发细胞死亡。
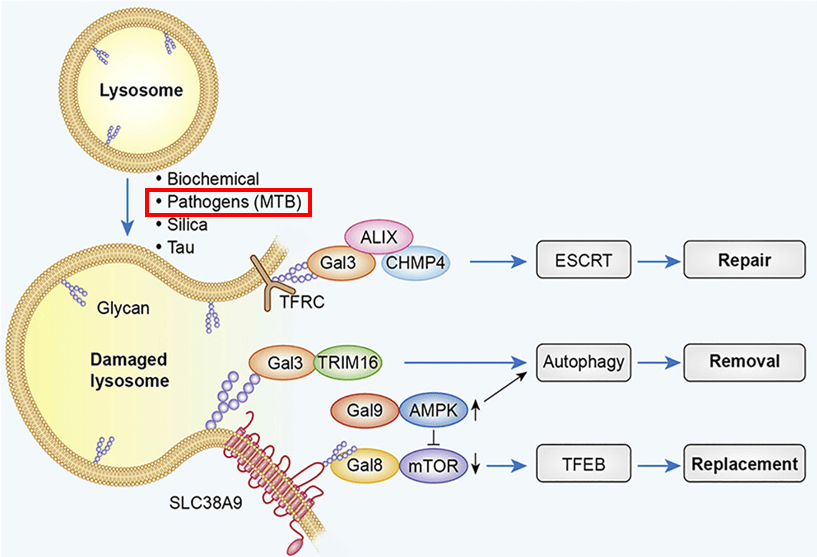
酶体膜损伤后的修复、移除和替换[4]
细胞在应对溶酶体损伤时采用多种机制进行修复和维持细胞稳态[4]。转运必需内体分选复合物(Endosomal Sorting Complex Required for Transport, ESCRT)可以修复受损的溶酶体膜;自噬(Autophagy)可以清除受损的溶酶体;转录因子EB(Transcription Factor EB,TFEB) 的激活促进溶酶体生成和水解酶合成,加速溶酶体的更新。
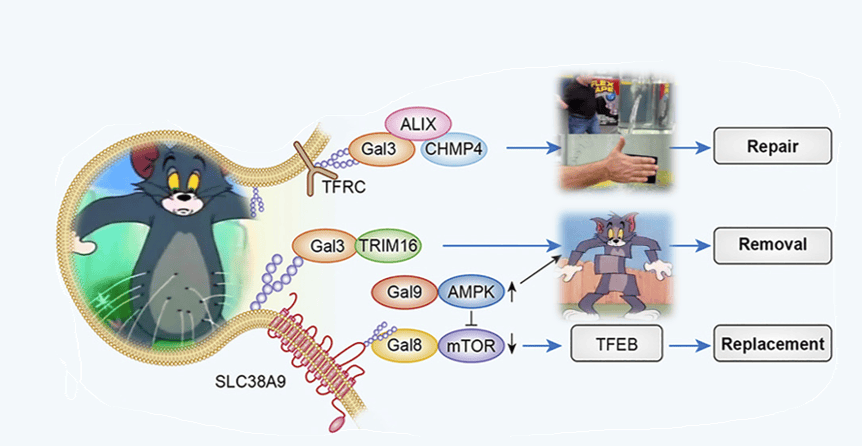
Repair or Remove?这是个问题
溶酶体膜受损后的命运受多种因素影响,包括损伤程度和性质、细胞状态、ESCRT复合体活性、自噬调控以及外部环境条件等。轻微损伤可能触发修复机制,而严重损伤可能导致清除受损溶酶体。资源充足的环境可能更有利于修复,而资源匮乏或压力较大的环境则可能促使细胞选择清除受损溶酶体。
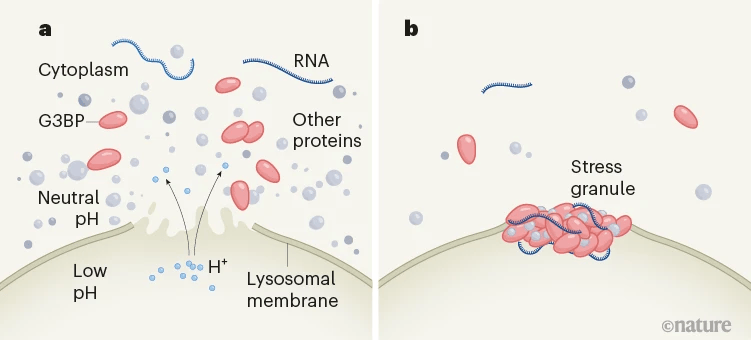
应激颗粒为渗漏的溶酶体提供急救[5]
最近,Maximiliano G. Gutierrez团队[6]发现应激颗粒可以在溶酶体膜受损部位迅速凝聚,就像给伤口贴上超级坚固的“创可贴”,堵住膜上的小洞,阻止溶酶体内的物质外泄,维持溶酶体和细胞内部环境的稳定性,有利于溶酶体修复工作的开展。
应激颗粒是一种无膜细胞器,由RNA和蛋白质通过液-液相分离过程自发凝聚而成,犹如水中凝聚的油滴。Ras GTP酶激活蛋白相互作用蛋白(Ras GTPase-activating protein-binding protein, G3BP)是应激颗粒形成的关键因子,也可以作为应激颗粒的标志物。
Gutierrez团队[6]发现,pH值的下降可以触发G3BP1与RNA的凝聚,在损伤部位初步形成分子塞,随后发生膜浸润(membrane wetting),沿着囊泡膜表面扩散,进一步促进膜的稳定和修复。在巨噬细胞和小鼠模型中,结核分枝杆菌感染引发了溶酶体相关应激颗粒的形成;而在G3BP敲除的巨噬细胞中,溶酶体在急性损伤后的恢复能力下降,结核分枝杆菌的复制能力则显著增强。这表明应激颗粒在结核分枝杆菌感染中发挥了一定的抵抗作用,可能有助于限制病菌的复制和传播。
全球结核病疫情形式仍然严峻,到2030年终止结核病流行是联合国可持续发展目标的卫生相关目标之一。结核分枝杆菌是引起结核病的病原菌,会破坏宿主细胞中的溶酶体,导致细胞受损或死亡。最近的研究开创性地揭示了应激颗粒在溶酶体修复中的关键作用,为治疗结核病提供了新的思路和方法。未来,相信我们能够找到更有效的预防和治疗策略。
参考资料:
[1]. Witt M, Szklener A, Marchwica W, Dobosz T. Disease not genetic but infectious: multiple tuberculomas and fibrinous pericarditis as symptoms pathognomonic for tuberculosis of Frederic Chopin. J Appl Genet. 2018;59(4):471-473.
[2]. 结核病 (who.int)
[3]. 溶酶体 - 维基百科,自由的百科全书 (wikipedia.org)
[4]. Jia J, Claude-Taupin A, Gu Y, et al. Galectin-3 Coordinates a Cellular System for Lysosomal Repair and Removal. Dev Cell. 2020;52(1):69-87.e8.
[5]. Plassmeyer SP, Holehouse AS. Stress granules offer first aid for leaky organelles. Nature. 2023;623(7989):919-920.
[6]. Bussi C, Mangiarotti A, Vanhille-Campos C, et al. Stress granules plug and stabilize damaged endolysosomal membranes [published correction appears in Nature. 2023 Nov 22;:]. Nature. 2023;623(7989):1062-1069.
撰稿:闫润
审核:Genes & Diseases 新媒体
